Câu hỏi: Chọn phương án đúng. Cho quá trình điện cực: 3Fe3+(dd) + 4H2O(ℓ) + 1e → Fe3O4(r) + 8H+(dd). Phương trình Nerst đối với quá trình đã cho ở 250C có dạng:
A. \(\varphi = {\varphi ^0} + 0.059\lg \frac{{{{\left[ {{H^ + }} \right]}^8}}}{{{{\left[ {F{e^{3 + }}} \right]}^3}{{\left[ {{H_2}O} \right]}^4}}}\)
B. \(\varphi = {\varphi ^0} + 0.059\lg \frac{{{{\left[ {{H^ + }} \right]}^8}}}{{{{\left[ {F{e^{3 + }}} \right]}^3}}}\)
C. \(\varphi = {\varphi ^0} + 0.059\lg \frac{{{{\left[ {F{e^{3 + }}} \right]}^3}}}{{{{\left[ {{H^ + }} \right]}^8}}}\)
D. \(\varphi = {\varphi ^0} + 0.059\lg \frac{{{{\left[ {F{e^{3 + }}} \right]}^3}{{\left[ {{H_2}O} \right]}^4}}}{{\left[ {F{e_3}{O_4}} \right]{{\left[ {{H^ + }} \right]}^8}}}\)
Câu 1: Chọn phương án đúng: Cho phản ứng: H3PO4 + 2NaOH = Na2HPO4 + 2H2O. Đương lượng gam của H3PO4 và NaOH lần lượt bằng: (Cho biết phân tử gam của H3PO4 bằng 98g và của NaOH bằng 40g)
A. 98g ; 40g
B. 32,7g ; 40g
C. 49g; 40g
D. 98g ; 20g
30/08/2021 1 Lượt xem
Câu 2: Chọn trường hợp đúng. Biết rằng nhiệt tạo thành tiêu chuẩn của AsH3 (k), NH3(k), PH3 (k) và C2H4 (k) lần lượt bằng: 66,44 ; -46,11; 5,4 ; 52,26 (kJ/mol). Trong 4 chất này, chất dễ bị phân hủy thành đơn chất nhất là:
A. C2H4
B. PH3
C. AsH3
D. NH3
30/08/2021 1 Lượt xem
Câu 3: Chọn phương án đúng: Cho các số liệu sau: (1) jo (Al3+/Al) = - 1,706 V ; (2) jo (Zn2+/Zn) = - 0,764 V ; (3) jo (Cu2+/Cu+) = + 0,15 V ; (4) jo (Cu+/Cu) = + 0,522 V. Các chất được sắp xếp theo thứ tự tính oxy hóa tăng dần như sau:
A. Al3+ < Zn2+ < Cu2+ < Cu +
B. Cu + < Cu 2+ < Zn2+ < Al3+
C. Al < Zn < Cu + < Cu
D. Cu < Cu + < Zn < Al
30/08/2021 1 Lượt xem
Câu 4: Chọn trường hợp đúng. Quá trình đông đặc nước đá ở -1°C và 1 atm có:
A. DS < 0, DH < 0, DG < 0
B. DS < 0, DH < 0, DG > 0
C. DS < 0, DH > 0, DG < 0
D. DS >0, DH < 0, DG < 0
30/08/2021 1 Lượt xem
Câu 5: Chọn phương án đúng: Cho giản đồ hòa tan như hình sau: 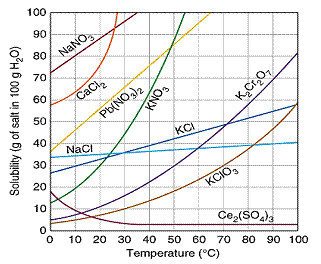
A. Không đủ cơ sở để xác định
B. Dung dịch chưa bão hòa
C. Dung dịch bão hòa
D. Dung dịch quá bão hòa
30/08/2021 2 Lượt xem
Câu 6: Chọn phương án đúng: Cho cân bằng CO2(k) + H2(k) ⇄ CO(k) + H2O(k). Tính hằng số cân bằng Kc của phản ứng. Biết rằng phản ứng được thực hiện trong bình kín có dung tích 1 lít chứa 0,3 mol CO2 và 0,3 mol H2 lúc ban đầu. Khi phản ứng cân bằng ta có 0,2 mol CO tạo thành. Nếu nén hệ cho thể tích của hệ giảm xuống, cân bằng sẽ chuyển dịch như thế nào?
A. Kc = 8 ; theo chiều nghịch
B. Kc = 8 ; theo chiều thuận
C. Kc = 4 ; không đổi
D. Kc = 4 ; theo chiều thuận
30/08/2021 1 Lượt xem

Câu hỏi trong đề: Bộ câu hỏi trắc nghiệm môn Hóa học đại cương - Phần 10
- 1 Lượt thi
- 50 Phút
- 45 Câu hỏi
- Sinh viên
Cùng chủ đề Bộ câu hỏi trắc nghiệm môn Hóa học đại cương có đáp án
- 652
- 19
- 45
-
62 người đang thi
- 694
- 3
- 45
-
10 người đang thi
- 672
- 7
- 45
-
85 người đang thi
- 625
- 2
- 45
-
50 người đang thi




Chia sẻ:
Đăng Nhập để viết bình luận