Câu hỏi: Trước đây, người ta không không rõ ion thủy ngân (I) tồn tại trong dung dịch dưới dạng \(Hg_n^{n + }\) với giá trị n bằng bao nhiêu. Để xác định n, có thể lập một pin như sau ở 25oC. Pt, Hg(ℓ)| dd A|| dd B| Hg(ℓ), Pt. 1 lít dung dịch A chứa 0,263g Hg(I) nitrat và 1 lit dung dịch B chứa 2,630g Hg(I) nitrat. Sức điện động đo được là 0,0289 V. Hãy xác định giá trị của n.
A. n = 3
B. n = 4
C. n = 1
D. n = 2
Câu 1: Hãy xác định ở giá trị nào của pH thì phản ứng sau bắt đầu xảy ra theo chiều thuận ở 25oC. HAsO2(dd) + I2(r) + 2H2O(ℓ) ⇄ H3AsO4(dd) + 2I- (dd) + 2H+ (dd). Cho biết, ở 25oC: \varphi _{\left( {{H_3}As{O_4}/HAs{O_2}} \right)}^0 = + 0,559V ; \varphi _{\left( {{I_2}/{I^ - }} \right)}^0 = + 0,5355V. Nồng độ các chất: [H3AsO4]=[I-]=[HAsO2] = 1M
A. pH > 0,4
B. pH > 3,0
C. pH > 1,0
D. pH > 2,0
30/08/2021 1 Lượt xem
Câu 2: Chọn phương án đúng: Cho phản ứng oxy hóa khử: HI + H2SO4 = I2 + S + H2O. Cân bằng phản ứng trên. Nếu hệ số trước H2SO4 là 1 thì hệ số đứng trước HI và I2 lần lượt là:
A. 2 và 1
B. 6 và 3
C. 8 và 4
D. 4 và 2
30/08/2021 1 Lượt xem
Câu 3: Chọn phương án đúng: Cho giản đồ hòa tan như hình sau: 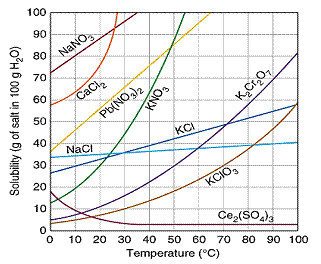
A. Không đủ cơ sở để xác định
B. Dung dịch chưa bão hòa
C. Dung dịch bão hòa
D. Dung dịch quá bão hòa
30/08/2021 2 Lượt xem
Câu 4: Chọn phát biểu đúng: Phản ứng A (k) ⇄ B (k) + C (k) ở 300oC có Kp = 11,5; ở 500oC có Kp = 23. Tính ∆Ho của phản ứng trên. Cho R = 8,314 J/mol.K.
A. DHo = + 4,32 kJ
B. DHo = + 12,76 kJ
C. DHo = -12,76 kJ
D. DHo = - 4,32 kJ
30/08/2021 1 Lượt xem
Câu 5: Chọn phương án đúng: Ở 25°C, áp suất hơi bão hòa của nước nguyên chất là 23,76mmHg. Khi hòa tan 2,7mol glyxerin vào 100mol H2O ở nhiệt độ trên thì độ giảm tương đối áp suất hơi bão hòa của dung dịch so với nước nguyên chất bằng:
A. 0,026
B. 0,042
C. 0,974
D. 0,625
30/08/2021 1 Lượt xem
Câu 6: Chọn phương án đúng: Nhỏ từng giọt dung dịch (NH4)2C2O4 0,01M vào 1 lít dung dịch chứa 1 ion gam Ba2+ và 0,005 ion gam Ca2+ . Hỏi kết tủa nào xuất hiện trước? (Cho tích số tan của BaC2O4 và CaC2O4 lần lượt bằng 10-6,96 và 10-8,64).
A. Cả 2 kết tủa xuất hiện cùng lúc
B. BaC2O4
C. CaC2O4
D. Không xác định được
30/08/2021 1 Lượt xem

Câu hỏi trong đề: Bộ câu hỏi trắc nghiệm môn Hóa học đại cương - Phần 10
- 1 Lượt thi
- 50 Phút
- 45 Câu hỏi
- Sinh viên
Cùng chủ đề Bộ câu hỏi trắc nghiệm môn Hóa học đại cương có đáp án
- 653
- 19
- 45
-
70 người đang thi
- 696
- 3
- 45
-
40 người đang thi
- 674
- 7
- 45
-
60 người đang thi
- 626
- 2
- 45
-
62 người đang thi




Chia sẻ:
Đăng Nhập để viết bình luận