Câu hỏi:
Cho các nhận định sau:
1.Hg phản ứng với S ngay ở nhiệt độ thường.
2.Trong công nghiệp, axit sunfuric được sản xuất theo phương pháp tiếp xúc gồm ba giai đoạn.
3.Khi sục khi H2S vào dung dịch NaOH có thể thu được hai loại muối: Na2S và NaHS.
4.Axit sunfuric loãng không thể hiện tính oxi hóa.
5.Khi sục khí SO2 từ từ đến dư vào dung dịch Ba(OH)2 thì thấy có kết tủa trắng xuất hiện.
6.Ozon có tính oxi hóa mạnh hơn oxi do nó có thể tan trong nước tốt hơn oxi.
Số nhận định không đúng là
A. 2
B. 3
C. 4
D. 5
Câu 1: Khi cho Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng thì sản phẩm thu được là
A. Fe2(SO4)3, SO2 và H2O.
B. Fe2(SO4)3 và H2O.
C. FeSO4, SO2 và H2O.
D. FeSO4 và H2O.
17/11/2021 2 Lượt xem
Câu 2: Cho dãy các kim loại: Zn, Al, Cu, Fe, Ag. Số kim loại trong dãy phản ứng được với dung dịch H2SO4 loãng là:
A. 5
B. 2
C. 4
D. 3
17/11/2021 1 Lượt xem
Câu 3: Dùng thuốc thử nào sau đây để có thể phân biệt được các dung dịch NaOH, Ba(OH)2, H2SO4, NaCl?
A. Quỳ tím.
B. dung dịch BaCl2.
C. dung dịch AgNO3.
D. dung dịch Na2CO3.
17/11/2021 1 Lượt xem
Câu 4: Trường hợp nào sau đây xảy ra phản ứng hóa học?
A. Cho Cu vào dung dịch H2SO4 loãng
B. Sục khí H2S vào dung dịch Pb(NO3)2
C. Sục khí H2S vào dung dịch FeCl2
D. Cho Al vào dung dịch H2SO4 đặc nguội
17/11/2021 1 Lượt xem
Câu 5: Cho phản ứng của sắt với oxi như hình vẽ sau:
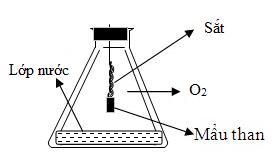
Vai trò của lớp nước ở đáy bình là

A. giúp cho phản ứng của sắt với oxi xảy ra dễ dàng hơn.
B. hòa tan oxi để phản ứng với sắt trong nước.
C. tránh vỡ bình vì phản ứng tỏa nhiệt mạnh và oxit sắt có thể rơi xuống đáy.
D. Cả 3 vai trò trên.
17/11/2021 1 Lượt xem
Câu 6: Cho 0,2 mol SO2 tác dụng với 0,3 mol NaOH, sau phản ứng thu được m gam muối. Giá trị của m là
A. 18,9g.
B. 23g.
C. 20,8g.
D. 24,8g.
17/11/2021 2 Lượt xem

Câu hỏi trong đề: Đề thi giữa HK2 môn Hóa học 10 năm 2021 của Trường THPT Hoa Lưu A
- 0 Lượt thi
- 50 Phút
- 40 Câu hỏi
- Học sinh
Cùng danh mục Thư viện đề thi lớp 10
- 763
- 1
- 40
-
85 người đang thi
- 708
- 1
- 40
-
85 người đang thi
- 814
- 1
- 40
-
71 người đang thi
- 772
- 0
- 40
-
97 người đang thi




Chia sẻ:
Đăng Nhập để viết bình luận